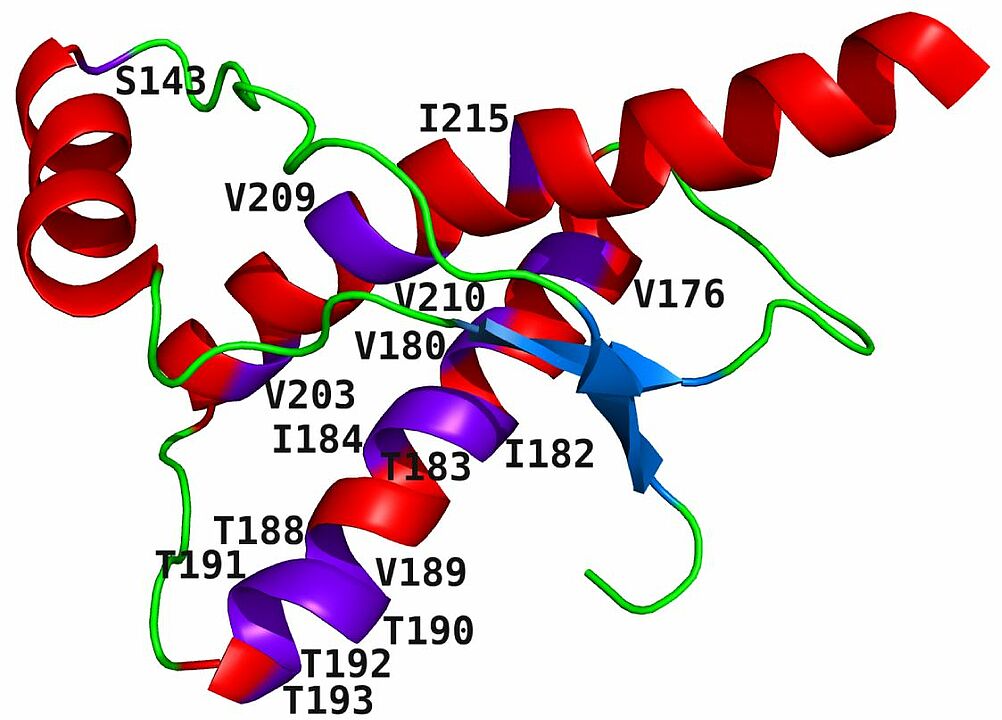
Nehmen PrP und Abeta eine unkorrekte Faltung an und bilden sie unlösliche Aggregate, so wirken sie zerstörerisch auf Nervenzellen. Die beiden Proteine können allerdings auch miteinander wechselwirken und dadurch ihre zerstörerische Wirkung potenzieren: Wenn zellschädigende Zusammenlagerungen (sogenannte Oligomere) aus Abeta – das in seiner monomeren Form unschädlich ist – sich an zellgebundenes PrP binden, kann dies toxische Signalwege aktivieren. Die Wechselwirkung kann aber auch die toxische Wirkung der Proteine abschwächen – dann nämlich, wenn lösliches PrP oligomeres Abeta einhüllt und dadurch unschädlich macht.
Diese Wechselwirkung zwischen PrP und Abeta haben die Wissenschaftlerinnen und Wissenschaftler aus Düsseldorf und Jülich sichtbar gemacht. Dazu untersuchten sie mithilfe hochauflösender Festkörper-NMR-Spektroskopie Komplexe dieser beiden Proteine. Das Ergebnis: Das Prion-Protein bleibt bei der Bindung an Abeta weitgehend ungefaltet. Nur das C-terminale Ende, das nicht an der Bindung beteiligt ist, ändert seine Struktur, was ein Hinweis auf seinen Beitrag zum toxischen Signalweg sein kann. Die Abeta-Aggregate dagegen sind heterogen und zeigen schon deutliche Ähnlichkeiten mit verschiedenen möglichen Spätformen, den Amyloidfibrillen, auf.
Für die Untersuchungen wurden modernste Lösungs- und Festkörper-NMR-Spektrometer am biomolekularen NMR-Zentrum der HHU am Forschungszentrum Jülich genutzt.
Originalpublikation
König AS, Rösener NS, Gremer L, Tusche M, Flender D, Reinartz E, Hoyer W, Neudecker P, Willbold D, Heise H, Structural details of amyloid β oligomers in complex with human prion protein as revealed by solid-state MAS NMR spectroscopy, Journal of Biological Chemistry (2021)